Vorwort
ACHTUNG! In diesem eBook werden verschiedene Medikamente beschrieben. Meine Absicht ist dabei, u.a. die Wirkung dieser Medikamente und ihren Einsatz so zu erklären, daß auch medizinische Laien sie verstehen. Es handelt sich nicht um eine genaue Betriebsanleitung, sodaß alle hier gemachten Angaben unverbindlich sind und keinesfalls als genaue Segelanleitung verstanden werden dürfen. Mit anderen Worten:
Wenn der Leser den Inhalten dieses eBooks folgt und hierdurch einen Schaden erleidet hafte ich nicht für diesen Schaden. Das eBook dient lediglich zur Information.
Einleitung
Damit Sie verstehen können, was Marcumar® und die anderen Medikamente zur Hemmung der Blutgerinnung bewirken, sollten Sie zunächst wissen, wozu die Blutgerinnung dient.
Der Zweck der Blutgerinnung
 |
| Abb.1 |
Die Blutgerinnung ist ein lebensnotwendiger Vorgang: Infolge kleinerer oder größerer Verletzungen kommt es an der Haut oder auch im Inneren des Körpers immer wieder zu Blutungen. Die Blutungen aus Verletzungen der Haut, wenn man sich z.B. geschnitten oder gestochen hat, sind jedermann bekannt. Auch der blaue Fleck an Stellen, an denen man sich heftig gestoßen hat, ist auf eine Blutung zurückzuführen, die aber innerhalb der Haut und des Gewebes unterhalb der Haut stattfindet.
Wenn man sich beispielsweise den Kopf heftig stößt kann es aber auch Verletzungen der Blutgefäße innerhalb des Körpers, z.B. im Schädel und im Gehirn geben. Auch aus diesen Gefäßverletzungen kann es bluten, man spricht dann von „inneren Blutungen“.
Und schließlich kann es auch ohne direkten Anlass innerhalb des Körpers zu Blutungen kommen. Solche „Spontanblutungen“ treten beispielsweise auf, wenn der Blutdruck sehr stark ansteigt und die Blutgefäße dadurch „platzen“.
Blutungen, von denen ich oben geschrieben habe, gefährden die Funktion des Körpers. Aus schweren Verletzungen der Haut kann man verbluten, aber auch „innere Blutungen“ etwa in den Bauch oder in das Gehirn können verheerende oder sogar tödliche Folgen haben. Aus diesem Grund benötigt der Körper das Blutgerinnungssystem, um Undichtigkeiten der Blutgefäße abzudichten und äußere oder innere Blutungen zu verhindern.
Dabei erfolgt die Abdichtung des verletzten Blutgefäßes durch einen kleinen Blutpfropf (sog. Thrombus oder Blutgerinnsel), der das Leck abdichtet (man kennt solche Blutgerinnsel an äußeren Verletzungen der Haut).
Ablauf der Blutgerinnung
Zweck der Blutgerinnung ist die Bildung von Blutgerinnseln (Thromben), die eine Undichtigkeit in der Wand von Blutgefäßen abdichten soll. Zuständig hierfür ist das Gerinnungssystem des Körpers. Man unterteilt den Ablauf der Blutgerinnung in 4 Stufen:
- Zu Beginn der Gerinnung, in Stufe 1, kommt es zu einer Zusammenballung von Blutplättchen (Thrombozyten) zu einem winzigen Pfropfen.
Er entsteht an einer Stelle der Gefäßinnenhaut (Endothel), die z.B. durch Diabetes, Bluthochdruckkrankheit oder Rauchen geschädigt ist oder bei der die Gefäßwand einreißt.
Ausgelöst durch eine solche Schädigung wird ein spezieller Eiweißkörper, der sog. von-Willebrand-Faktor von den Zellen der Gefäßinnenhaut (Endothel-Zellen) und von bestimmten Blutkörperchen (Megakaryozyten = Vorläuferzellen der Blutplättchen) gebildet und ausgeschüttet.
Kommt es zu einem Riss der Innenwand des Gefäßes, werden die darunter liegenden Strukturen der Gefäßwand freigelegt, u.a. das Kollagen.
An dieses Kollagen kann sich der Von-Willebrand-Faktor ankoppeln.
Die Blutplättchen (Thrombozyten) verfügen auf ihrer Oberfläche ebenfalls eine Andockstelle für den von-Willebrand-Faktor. Indem sich der von-Willebrand-Faktor sowohl mit dem Kollagen als auch mit den Thrombozyten verbindet schafft er eine Brücke zwischen den Blutplättchen und der verletzten Gefäßwand.
Diese Verbindung zwischen den Blutplättchen und dem Kollagen führt zu einer Aktivierung der Thrombozyten. Diese Aktivierung hat an den Thrombozyten mehrere Auswirkungen:
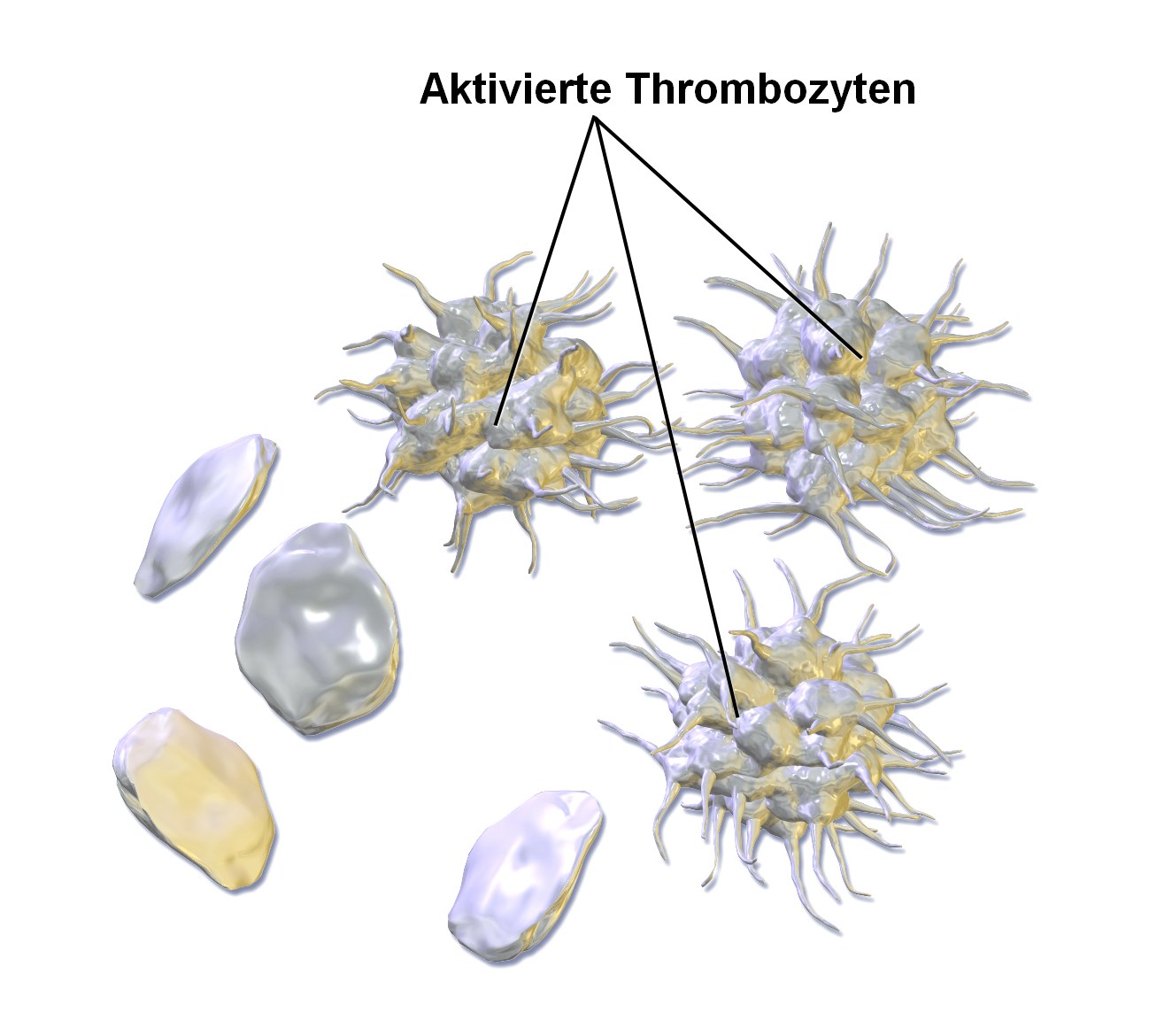
Abb.2 Thrombozyten links: Inaktive, rechts :aktive Blutplättchen Zu finden im Internet unter: https://commons.wikimedia.org/wiki/File:Blausen_0740_Platelets-de.jpg - Sie ändern ihr Aussehen: Nicht aktivierte Thrombozyten sind winzige unregelmäßig runde Zellen ohne einen Zellkern (Abb. 2).
Durch die Aktivierung der Thrombozyten bilden sie zahlreiche Ausstülpungen und vergrößern so ihre Oberfläche um ein Mehrfaches.
- Gleichzeitig setzen sie bestimmte Substanzen frei, die zuvor in ihrem Inneren produziert worden sind: U.a. ADP (Adenosin-di-phosphat) und Thromboxan.
Die Synthese des Thromboxans erfolgt dabei mit Hilfe des Enzyms Cyclooxidase (COX).
Auf der Oberfläche der Thrombozyten befinden nun Andockstellen (Rezeptoren) sowohl für Thromboxan als auch für ADP (P2Y12-Rezeptor).
- Werden diese Rezeptoren mit ADP bzw. Thromboxan besetzt und damit aktiviert kommt es zu einer weiteren Verstärkung der Thrombozytenaktivierung. Dies hat ebenfalls 2 wichtige Auswirkungen:
- An der Oberfläche der Thrombozyten befinden sich neben den schon erwähnten Rezeptoren zusätzlich Bindungsstellen für Fibrinogen, einen wichtigen Gerinnungsfaktor (siehe unten).
Dieser Fibrinogen-Rezeptor wird nun ebenfalls aktiviert, was dazu führt, daß sich die einzelnen aktivierten Thrombozyten mit anderen Thrombozyten verbinden, sodaß ein starkes quervernetztes Geflecht entsteht.
- Die verstärkte Thrombozytenaktivierung führt aber zusätzlich dazu, daß sich an der Oberfläche der Thrombozyten nun die aktivierten Gerinnungsfaktoren 10a und 5a (siehe unten) anlagern können.
Diese Faktoren wiederum führen zur Umwandlung von Prothrombin zu Thrombin, das dann wiederum Fibrinogen in Fibrin umwandelt.
Die Fibrin-Fäden zusammen mit den vernetzten aktivierten Thrombozyten (siehe oben) ein Netzwerk aus Fäden, in dem sich andere Bestandteile des Blutes, z.B. die roten Blutkörperchen (Erythrozyten) verfangen.
- An der Oberfläche der Thrombozyten befinden sich neben den schon erwähnten Rezeptoren zusätzlich Bindungsstellen für Fibrinogen, einen wichtigen Gerinnungsfaktor (siehe unten).
- Sie ändern ihr Aussehen: Nicht aktivierte Thrombozyten sind winzige unregelmäßig runde Zellen ohne einen Zellkern (Abb. 2).
- In Stufe 2 der Blutgerinnung kommt es zur Bildung des eigentlichen Blutgerinnsels.
Es entsteht dadurch, daß verschiedene Gerinnungsfaktoren des Blutes aus ihrer inaktiven Form in die aktive Form überführt werden.
Die Gerinnungsfaktoren werden dabei einfach durchnummeriert, wobei die aktiven Faktoren mit ihrer Zahl und dem Anhängsel „a“ bezeichnet werden.
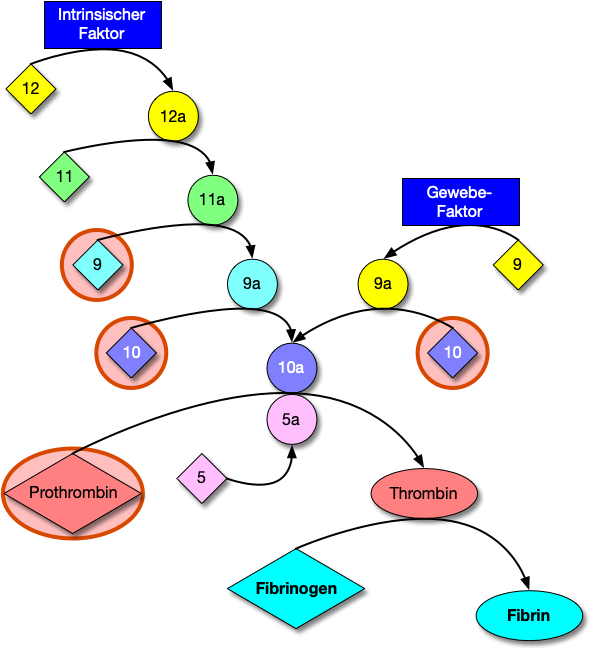
Abb.3 Besondere Bedeutung haben im Zusammenhang dieses eBook über gerinnungshemmende Medikamente die Faktoren 2, 7, 9 und 10.
Ebenso wie die anderen Gerinnungsfaktoren werden sie in der Leber gebildet, benötigen aber zur Herstellung Vitamin K, was für die Wirkung von Marcumar® (siehe später) wichtig ist.
Das Ganze läuft dann wie eine Kettenreaktion ab, indem ein aktivierter Faktor einen weiteren noch inaktiven Faktor in seine aktive Form überführt, der dann seinerseits wiederum den nächsten Faktor aktiviert (Abb. 3).
Diesen Ablauf bezeichnet man als Gerinnungskaskade.
Man unterscheidet dabei eine von innen (intrinsische) und eine von außen (extrinsische) ausgelöste Kaskade.
Die extrinsische Kaskade wird durch den sog. Gewebefaktor ausgelöst.
Dieser Faktor befindet sich in den Zellmembranen von Geweben, die direkt unterhalb des Gefäßinnenhäutchen liegen. Der Faktor wird durch Schädigungen des Endothels aktiviert, also immer dann, wenn diese Gewebe mit dem Blut (z.B. an einer eingerissenen Gefäßwand) in Verbindung kommt.
Dieser Gewebefaktor aktiviert dann den Gerinnungsfaktor 7 und aktiviert ihn. Der aktivierte Faktor 7 wiederum aktiviert seinerseits den Gerinnungsfaktor 10.
Die intrinsische Kaskade wird durch aktivierte Blutplättchen ausgelöst.
Es kommt zur stufenweisen Aktivierung der Gerinnungsfaktoren 12, 11, 9 und 10. In der Aktivierung des Faktor 10 berühren sich die extrinsische und die intrinsische Kaskade.
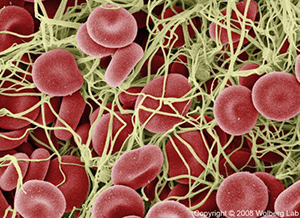
Abb.3 Dieser aktivierte Faktor 10 schließlich überführt einen weiteren inaktiven Blutfaktor (Prothrombin) in seine aktive Form, das Thrombin, das dann wiederum den letzten Schritt der Blutgerinnung, die Umwandlung von Fibrinogen in Fibrin auslöst.
Fibrinogen ist eine im Blut lösliche Substanz, Fibrin jedoch ein fadenförmiges, nicht mehr blutlösliches chemisches Gebildet. An der Verletzungsstelle entsteht ein ganzes Geflecht solcher Fibrinfäden, in denen sich Blutkörperchen verfangen (Abb. 4).
Dies ist das eigentliche Blutgerinnsel.
Auf diese Weise entsteht ein Blutpfropf (= Blutgerinnsel = Thrombus). Idealerweise dichtet dieser Thrombus die undichte Gefäßstelle ab, wenn die Gefäßinnenhaut aber „nur“ geschädigt, jedoch nicht gerissen ist, entsteht das Gerinnsel im Innenraum des Gefäßes.
- In Stufe 3 der Gerinnung ist die Bildung eines Blutgerinnsels abgeschlossen und es beginnen nun Vorgänge, die den Thrombus wieder auflösen.
Hierbei spielt eine Substanz mit Namen Antithrombin eine Rolle.
Antithrombin wird in der Leber gebildet und hat die Eigenschaft, sich an das Thrombin, das bereits im Ablauf der Blutgerinnung entstanden ist, anzuhaften und es aufzulösen. Dadurch verhindert es die Umwandlung von Fibrinogen zu Fibrin (siehe Abb. 2) und ist damit ein Hemmstoff der Blutgerinnung.
Die Verbindung von Antithrombin und Thrombin verläuft langsamer als die Aktivierung des Fibrinogen zum Fibrin, weshalb es den Vorgang einer Gerinnselbildung selber nicht aufhält.
Der Sinn des Antithrombins besteht darin, eine zu starke Gerinnselbildung zu verhindern und letztlich dafür zu sorgen, daß das verletzte Blutgefäß nach außen abgedichtet wird, die Durchgängigkeit des Gefäßes für fließendes Blut aber erhalten bleibt. Die Steuerungs-Mechanismen des Antithrombins sind auch heute noch nicht bekannt.
- In der 4. Stufe des Gerinnungssystems schließlich kommt es zur Auflösung des Gerinnsels, wenn es nicht mehr benötigt wird.
Verantwortlich hierfür ist eine Substanz namens Plasmin.
Plasmin entsteht aus einer inaktiven Vorstufe, dem Plasminogen, das in der Leber gebildet und ins Blut freigesetzt wird. Seine Aktivierung und damit die Umwandlung von Plasminogen in Plasmin wird u.a. durch Fibrin und einen sog. Gewebs-Plasminogen-Aktivator ausgelöst.
Plasmin spaltet die Fibrinfäden des Gerinnsels in kleine Bruchstücke und löst den Thrombus damit auf, was man mit dem Begriff Fibrinolyse bezeichnet.
Die Bildung eines Gerinnsels und seine Auflösung laufen gleichzeitig ab. Dabei hat die Gerinnselbildung zu Beginn die Oberhand. Mit zunehmender Verheilung der Gefäßschädigung nimmt ihre Intensität allerdings kontinuierlich ab und die Fibrinolyse gewinnt nun die Oberhand, sodaß der Thrombus nach einer gewissen Zeit wieder verschwindet.
Im Zusammenhang mit diesem eBook, das sich mit gerinnungshemmenden Medikamenten beschäftigt, werde ich auf die Stufe 4 nicht näher eingehen, weil sie hier keine bedeutsame Rolle spielen.
Gerinnungshemmende Medikamente
Es gibt verschiedene gerinnungshemmende Medikamente (Antikoagulantien), die an verschiedenen Stellen der oben beschriebenen Gerinnungskaskade eingreifen: Die einen blockieren einige der oben genannten Gerinnungsfaktoren, andere wirken zusammen mit dem Antithrombin und wiederum andere hemmen die Bildung von Gerinnungsfaktoren in der Leber.
Besprechen möchte ich vielmehr Medikament, die in den Stufen 1, 2 und 3 der Gerinnungskaskade eingreifen:
- Heparin
- Thrombozytenaggregationshemmer
- Marcumar® und
- nicht-Vitamin K-abhängige Medikamente (DOAK)
Gründe zur Gerinnungshemmung
Gerinnungshemmende Medikamenten werden aus zahlreichen Gründen eingesetzt, wie Sie im nächsten Abschnitt lesen werden. Welches der verschiedenen Medikamente man einsetzt hängt von der Art der Erkrankung, von den Risiken der verschiedenen Medikamente und vom Zustand des Patienten ab.
Was die medizinischen Gründe angeht werden Antikoagulantien am häufigsten eingesetzt bei
- Vorhofflimmern
- Venenthrombosen und
- künstlichen mechanischen Herzklappenprothesen
Nachfolgend finden Sie eine Aufstellung, bei welchen Krankheiten Gerinnungshemmer eingesetzt werden. Dabei wird auch erwähnt, welches Medikament in der jeweiligen Situation eingesetzt wird. Die Medikamente selber werden in späteren Kapiteln besprochen.
Vorhofflimmern
Hier wird ein DOAK eingesetzt, um zu verhindern, daß sich Gerinnsel im „Ohr“ des linken Vorhofs bilden.
Solche Gerinnsel bei Vorhofflimmern sind eine Quelle für Hirnembolien mit hierdurch bedingtem Schlaganfall.
Beinvenenthrombose
Eingesetzt werden DOAKs, um die Auflagerung frischer Gerinnsel auf einen schon in der Vene liegenden Thrombus zu verhindern und einer Loslösung dieser frischen Thromben mit einer hieraus folgenden Lungenembolie zu verhindern.
Gerinnungshemmer werden nur bei Thrombosen in den tiefen, nicht in den oberflächlichen Beinvenen angewandt, weil nur Gerinnsel aus den tiefen Beinvenen gefährlich werden können.
Lungenembolie
Eine Gerinnungshemmung mit einem DOAK wird ebenfalls eingesetzt, wenn es zu einer Lungenarterienembolie gekommen ist und zwar unabhängig davon, ob man eine Emboliequelle hat nachweisen können oder nicht.
Mechanische Herzklappenprothese
Eingesetzt werden darf nur Marcumar® oder, wenn diese Behandlung unterbrochen werden muß, Heparin. DOAKs sind verboten, denn sie sind nicht verläßlich in der Lage, die Bildungen von Gerinnseln an und in den Klappen zu verhindern.
Ballonerweiterung (PTCA) mit oder ohne Stentimplantation
Hierbei muß wegen der Verletzung der Gefäßwand durch den PTCA-Ballon bzw. den Stent als „Fremdkörper“ mit dem Auftreten von Blutgerinnseln innerhalb der behandelten Herzkranzarterie gerechnet werden.
Daher wird während dieses Eingriffs Heparin und in der nachfolgenden Zeit ASS und ein „Super-Aspirin“ eingesetzt, wobei ASS und das „Super-Aspirin“ zunächst gleichzeitig genommen und dann zeitlich versetzt abgesetzt werden.
Akuter Herzinfarkt
Eingesetzt wird nur in der akuten Behandlung Heparin, um eine Größenzunahme des Thrombus in der Herzkranzarterie zu verhindern.
Nachfolgend werden ASS und ein „Super-Aspirin“ eingesetzt, wobei ebenso wie bei PTCAs und Stentimplantation ASS und das „Super-Aspirin“ zunächst gleichzeitig genommen und dann zeitlich versetzt abgesetzt werden.
Bei Patienten, die im Rahmen der Infarktbehandlung eine Ballonerweiterung gekommen haben oder denen ein Stent eingepflanzt worden ist, wird ebenso vorgegangen wie dies oben für PTCA und Stentimplantation beschrieben wurde.
Instabile Angina pectoris
Dieses Krankheitsbild, das eine Vorstufe zum Auftreten eines akuten Herzinfarktes darstellt, wird oft durch das Auftreten eines Blutgerinnsels im Inneren einer Herzkranzarterie hervorgerufen.
Eingesetzt wird Heparin, um eine Größenzunahme des Thrombus in der Herzkranzarterie zu verhindern.
Gerinnsel im linken Ventrikel
Bei einem nachgewiesenen Thrombus werden entweder Marcumar® oder ein DOAK eingesetzt, um zu verhindern, daß sich das Gerinnsel vergrößert, sich von der Wand losreißt und als Embolie in die Aorta schwimmt.
Man gibt es 3 - 4 Monate lang, weil der Thrombus nach dieser Zeit fest an den Ventrikelwand angewachsen ist.
Aneurysma (Aussackung) des linken Ventrikels
Solche Aussackungen entstehen meistens als Folge eines Herzinfarktes.
In einem Aneurysma kann es ebenfalls zur Entstehung von Thromben kommen, die, wenn sie sich losreißen, als Embolien (z.B. Hirnembolien) gefährlich werden können.
Eingesetzt wird in der Regel Marcumar®.
Verhütung von Gerinnselbildungen
Dies bezieht sich auf Situationen, in denen mit dem gehäuften Auftreten von Blutgerinnseln gerechnet werden muß, z.B. bei Operationen, Bettlägerigkeit oder Dialysebehandlung.
Eingesetzt wird hier in der Regel Heparin.
Verschiedene
Es gibt noch einige andere Gründe, gerinnungshemmende Medikamente einzusetzen (z.B. Venenthrombosen bei Tumorpatienten, vorbeugende Gerinnungshemmung bei Venenthrombosen o.ä.), auf die ich in diesem eBook aber nicht weiter eingehen möchte.
Verbotene Gerinnungshemmung
Absolut und ohne Ausnahme verboten ist der Einsatz gerinnungshemmender Medikamente wegen einer erhöhten Blutungsneigung bei
- aktiven Blutungen
- angeborenen oder erworbenen Blutgerinnungskrankheiten
- Operationen mit großem Blutungsrisiko, z.B. große Bauch-OP, OP an großen Schlagadern incl. der Aorta, große orthopädische OPs (z.B. Hüftgelenks-OP), große Operationen innerhalb des Blutkorbs, koronare Bypass-OP, Herzklappenersatz, Operationen am Gehirn oder der Wirbelsäule in der Nähe des Rückenmarks, Entfernung der Prostata, Entfernung der Harnblase oder Operation größerer Tumore
- akuter Blutung innerhalb des Schädels und
- größeren Verletzungen.
Abgewogen werden müssen Vorteile und Risiken einer Behandlung bei
- Magen-Darm-Blutungen
- mittelgroßen Operationen,
- Aussackungen oder Einrissen in der Aorta.
Vorsichtig benutzt sollten gerinnungshemmende Medikamente bei
- älteren Patienten und
- in der Schwangerschaft.
Hier ist in den ersten Monaten der Schwangerschaft Marcumar® verboten und sollte während dieser Zeit durch Heparin ersetzt werden. Auch im zeitlichen Zusammenhang mit der Entbindung sollte wegen der mütterlichen Blutungsgefahr eher Heparin eingesetzt werden.
Heparin
Wirkweise
Heparin wirkt nur im Zusammenspiel mit dem Antithrombin. Es bindet sich an Antithrombin und verstärkt dessen Wirkung tausendfach. Dadurch wird das Thrombin wesentlich schneller abgebaut, die Menge an Fibrin vermindert und damit die Bildung von Gerinnseln verhindert wird.
Heparin wirkt sehr schnell, wird aber auch schnell abgebaut, sodaß seine Wirkung schnell wieder verschwindet.
Medikamente
Man unterscheidet 2 verschiedene Heparine: Das unfraktionierte und das niedermolekulare Heparin.
Die Unterscheidung erfolgt aufgrund des „Gewichtes“ eines Heparin-Moleküls. Dabei hat das „natürliche“ Heparin, das der Körper in geringen Mengen selber produziert eine Molekularmasse von 6.000 - 30.000. Durch chemische Spaltung eines solchen Heparinmoleküls entstehen andere Heparine mit Molekularmassen um 5.000.
Das natürliche Heparin bezeichnet man als „Standard-„ oder unfraktioniertes Heparin, die gespaltenen Heparine nennt man niedermolekulares Heparin.
Sie unterscheiden sich nicht in ihrer Wirkweise, sondern in ihrer Wirkdauer, indem die niedermolekularen Heparine wesentlich länger wirken als die unfraktionierten Heparine.
Unfraktionierte Heparine (z.B. Liquemin®) werden eingesetzt, um kurzfristig zu wirken, indem man es z.B. als Infusion gibt. Die Stärke ihrer Wirkung muß laufend im Labor überprüft werden.
Niedermolekulare Heparine (z.B. Mono-Embolex® oder Clexane®) hingegen wirken auch längerfristig, indem man sie 1- oder 2mal täglich unter die Haut spritzt.
Die Wirkung dieser Heparine muß, außer in besonderen Situationen (z.B. Schwangerschaft oder Nierenfunktionsstörung) nicht kontrolliert werden.
Geschichte
Entdeckt wurde Heparin 1916 in Amerika. „Heparin“ wurde es genannt, weil es in der Leber (griechisch: hepar) vorkommt. Auch seine gerinnungshemmende Wirkung wurde bereits damals erkannt.
1937 wurde Heparin, das aus Rinderlungen und Schweinedärmen gewonnen wurde, erstmalig zur Behandlung einer tiefen Beinvenenthrombose und seit 1940 „routinemäßig“ zur Behandlung von auch anderen Erkrankung, bei denen es zu Thrombosen kommen konnte oder bei Embolien, eingesetzt.
Heparin wurde zunächst überwiegend aus tierischen Produkten, vor allem aus dem Gewebe von Rindern, gewonnen. Wegen einer rasanten Ausbreitung von BSE unter Rindern wurde die Heparin-Herstellung aber in den 1990er Jahren auf die Gewebe von Schweinen umgestellt.
m Verlauf der Covid-19-Pandemie und durch die Verbreitung der Schweinegrippe kam es aber zu einer massenhaften Schließung von Schlachthöfen, sodaß die Verfügbarkeit von unfraktioniertem Heparin stark abnahm.
Bereits in den 1970er Jahren entwickelte man die niedermolekularen Heparine, um die Nachteile des unfraktionierten Heparins, vor allem dessen nur kurze Wirkdauer, zu überwinden.
1980 wurde das erste niedermolekulare Heparin zugelassen und seit etwa 2000 werden diese Substanzen zunehmend eingesetzt.
Gründe für Heparin-Einsatz
- Tiefe Beinvenenthrombose
- Lungenembolie
- Vorhofflimmern
- Verhütung von Gerinnselbildungen z.B. bei Operationen, Bettlägerigkeit oder Dialysebehandlung
- instabile Angina pectoris
- frischer Herzinfarkt (mit oder ohne PTCA-Behandlung)
- Überbrückungs-Behandlung:
Bei Patienten, die mit Marcumar® oder einem DOAK behandelt werden müssen dauert es eine gewisse Zeit, bis diese Therapie wirksam wird.
Um die Patienten während dieser Zeit vor dem Auftreten von Gerinnseln zu schützen wird unfraktioniertes Heparin eingesetzt.
Dasselbe gilt für Patienten, deren Behandlung mit Marcumar® oder einem DOAK für eine gewisse Zeit unterbrochen werden muß (z.B. für eine Operation oder zu Beginn einer Schwangerschaft). Auch in solchen Situationen wird unfraktioniertes Heparin zur Überbrückung eingesetzt, Marcumar® setzt man z.B. 4 - 5 Tage vor einer Operation ab und gibt während dieser Zeit Heparin.
Wenn man später wieder Marcumar® geben darf setzt man die Heparin-Gabe solange fort, bis die Laborwerte zeigen, daß das Marcumar® wieder ausreichend wirksam ist.
Dosierung
Die Dosierung der verschiedenen Heparine ist abhängig
- von der Krankheit, deretwegen Heparin gegeben werden muß,
- von der Funktion von Leber und Niere,
- vom Lebensalter der Patienten (z.B. Kinder oder ältere Menschen),
- von der Art des Heparins, also unfraktioniertes oder niedermolekulares Heparin,
- von dem speziellen niedermolekularen Heparin, d.i. von demjenigen der verschiedenen Medikamente, das eingesetzt wird (also z.B. Enoxaparin oder Dalteparin)
- davon, ob die Patientin schwanger ist (Marcumar®-Verbot in den ersten 3 Monaten der Schwangerschaft und kurz vor der Entbindung)
- oder ob die Mutter das Kind mit der Brust stillt. Bei stillenden Müttern gelangt der Wirkstoff zwar in die Muttermilch, allerdings in so geringen Mengen, dass keine Nebenwirkungen beim Säugling zu erwarten sind. Eine pauschale Dosierungsempfehlung kann man daher nicht geben.
Lediglich beim Einsatz des unfraktionierten Heparins kann man sagen, daß es so dosiert werden muß, daß die PTT um das 1.5- - 2.0-fache des Normalwertes verlängert wird.
Nebenwirkungen
- Blutungen, z.B. Nasenbluten, winzige Hautblutungen (Petechien), Blut im Urin oder im Stuhl
- Reizungen an der Injektionsstelle
- Thrombozytopenie: Damit bezeichnet man eine Verminderung der Blutplättchen im Blut.
Diese Nebenwirkung tritt bei etwa 30% aller Menschen auf, die mit Heparin behandelt werden. Sie ist meistens harmlos, kann aber auch schwerwiegend sein. Man spricht dann von einer Heparin-induzierten Thrombozytopenie (HIT).
Eine HIT wird entweder durch eine immunologische Reaktion des Körpers ausgelöst oder stellt eine direkte Reaktion der Blutplättchen auf den Kontakt mit Heparin dar.
Die Thrombozytopenie als direkte Heparin-Nebenwirkung tritt 2 - 3 Tage nach Beginn einer Heparin-Dauertherapie auf und verschwindet nach dem Absetzen des Heparin wieder.
Die immunologisch verursachten Form tritt 5 Tage nach Beginn der Heparin-Dauertherapie auf und ist schwerwiegend, weil sie zum Auftreten von Thromben führen kann. Solche Thromben wiederum können eine tiefe Beinvenenthrombose, Lungenembolie, Schlaganfall, Herzinfarkt und Verstopfungen großer Schlagadern des Körpers mit Todesfolge oder Amputationsnotwendigkeit von Armen oder Beinen zur Folge haben.
Darf nicht gegeben werden bei
- Verminderung der Blutplättchen
- Patienten mit aktiver und noch nicht kontrollierter starker Blutung
- Patienten mit Heparin-induzierter Thrombozytopenie bei vorheriger Heparingabe
- Patienten ohne die Möglichkeit zur Laborkontrolle der Heparinwirkung
Überwachung
Die Wirkung des unfraktionierten Heparins muß mit bestimmten Laborwerten kontrolliert werden. Dazu benutzt eine bestimmte Blutungszeit (PTT = partielle Thromboplastinzeit). Je stärker das Heparin im Blut wirkt desto länger wird diese Zeit.
Man bestimmt den Wert in den ersten 2 Tagen einer Heparin-Dauertherapie etwa alle 6 - 12 Stunden, danach nur noch einmal täglich.
Der Wert der PTT, den man für eine effektive Behandlung anstrebt, ist eine Erhöhung auf das 1.5- bis 2-fache des Wertes, der für das jeweilige Blutlabor als Normalwert gilt.
Zusätzlich bestimmt man zur Erfassung einer evtl. Heparin-induzierten Thrombozytopenie einmal täglich die Anzahl der Blutplättchen im Blut.
Maßnahmen bei Überdosierung
Bei einer Überdosierung besteht die Gefahr, daß unkontrollierte, auch innere Blutungen auftreten.
Stellt man einen leicht bis mäßig erhöhten PTT-Wert fest genügt es in der Regel, die Heparingabe zu unterbrechen. Hat man zuvor unfraktioniertes Heparin gegeben wird sich die Blutgerinnung wegen der nur kurzen Wirkzeit dieses Heparins schnell wieder normalisieren.
Manchmal, z.B. im Zusammenhang mit bestimmten Operationen, muß man eine besonders große Heparinmenge geben. Um deren Wirkung sehr schnell, u.U. schon am Ende der Operation, wieder aufzuheben gibt man ein Medikament namens Protamin.
Es verbindet sich mit dem Heparin und inaktiviert es hierdurch.
Weil Protamin ein erhöhtes Risiko für das Auftreten auch schwerer allergischer Reaktionen hat darf es nur eingesetzt werden, wenn die apparativen und medikamentösen Voraussetzungen für einen unverzügliche Allergiebehandlung gegeben sind.
Thrombozytenaggregationshemmer
Wirkweise
Es gibt 2 Typen solcher Medikamente: Acetylsalicylsäure und ein „Super-Aspirin“.
Aspirin®
Acetylsalicylsäure blockiert innerhalb der Thrombozyten das Enzym Cyclooxidase (COX), das für die Herstellung von Thromboxan verantwortlich ist.
Thromboxan wiederum spielt eine wichtige Rolle bei der Aktivierung der Blutplättchen und der nachfolgenden Gerinnungskaskade.
Wenn also das Enzym COX blockiert wird entsteht weniger Thromboxan, die Blutplättchen werden nicht mehr aktiviert und der Ablauf der Gerinnung dadurch abgeschwächt.
Die Blockierung der COX durch die Acetylsalicylsäure ist unwiderruflich, COX kann in Thrombozyten nicht neu gebildet werden, denn diese haben keinen Zellkern, der für die Bildung einer neuen COX sorgen könnte. Daher sind die Thrombozyten für den Rest ihres 8- bis 12-tägigen Lebens auch nach kleinen Dosen von Acetylsalicylsäure vermindert funktionsfähig und können nur noch abgeschwächt an der Blutgerinnung mitwirken.
P2Y12-Hemmstoff („Super-Aspirin“)
Der Wirkstoff des „Super-Aspirins“ ist Clopidogrel.
Es blockiert die auf der Oberfläche der Thrombozyten gelegenen Rezeptoren für ADP (P2Y12-Rezeptor), weshalb dieses Medikament auch P2Y12-Hemmstoff genannt wird. Das Clopidogrel macht die Rezeptoren hierdurch funktionsunfähig.
ADP ist neben Thromboxan ein wichtiger Stoff, um die verstärkte Aktivierung der Thrombozyten auszulösen, wenn er sich an den ADP-Rezeptor auf der Thrombozytenoberfläche bindet. Wird dieser Rezeptor blockiert fällt ein Teil der verstärkten Thrombozytenaktivierung aus und die Blutgerinnung wird ebenfalls gehemmt.
Auch die Blockierung der ADP-Rezeptoren an der Thrombozytenoberfläche ist unwiderruflich, weil die Thrombozyten keine neuen Rezeptoren herstellen können.
Das ADP ist an der verstärkten Aktivierung der Thrombozyten stärker beteiligt als das Thromboxan, sodaß ein ADP-Blocker die Blutgerinnung stärker hemmt als ein Thromboxan-Blocker, daher die Bezeichnung „Super-Aspirin“ für das Clopidogrel.
Die gleichzeitige Gabe von Acetylsalicylsäure und Clopidogrel hemmt beide Wege der Blutgerinnung, was in besonderen Situationen ausgenutzt wird, in denen die Gerinnungshemmer intensiv sein muß (z.B. nach der Einpflanzung von Stents).
Medikamente
Acetylsalicylsäure z.B. Aspirin® oder ASS
Clopidogrel Plavix® oder Iscover®
Geschichte
Acetylsalicylsäure wurde früher aus der Weidenrinde gewonnen. Schon seit 4.000 Jahren war bekannt, daß es gegen Schmerzen und Fieber wirkt. 1899 wurde es von der Firma Bayer erstmals synthetisch hergestellt und unter der Bezeichnung Aspirin® verkauft und gegen Schmerzen und zur Fiebersenkung eingesetzt.
Daß Aspirin nicht nur gegen Schmerzen und Fieber wirkt, sondern auch Auswirkungen auf die Blutgerinnung hat, wurde erst in den 1970er-Jahren entdeckt. Seitdem wird das Medikament auch zur Gerinnungshemmung eingesetzt.
Gründe für den Einsatz
Für den Einsatz von Aspirin® (ASS) und „Super-Aspirin“ (SA) gibt es eine Vielzahl von Gründen. Ich führe nachfolgend nur diejenigen auf, die im Zusammenhang mit der Blutgerinnung stehen:
- Koronare Herzkrankheit (Aspirin®)
- Herzinfarkt, Vorbeugung (Aspirin®)
- Herzinfarkt, Behandlung mit PTCA/Stent (Aspirin® + „Super-Aspirin“)
- nach PTCA und/oder Stentimplantation (Aspirin® + „Super-Aspirin“)
- nach koronarer Bypass-Operation (Aspirin®)
- Schlaganfall, Vorbeugung (Aspirin®)
- nach Schlaganfall oder TIA (Aspirin® + „Super-Aspirin“)
Es gibt noch weitere Situationen, in denen einige Ärzte den Einsatz von Aspirin® erwägen, ohne daß dies aber allgemein akzeptiert wäre:
- nach Katheterimplantation der Aortenklappe (TAVI) (Aspirin®)
In der oben stehenden Aufstellung finden Sie häufiger „Aspirin® + „Super-Aspirin““. Diese Kombination bezeichnet man also duale Thrombozytenaggregationshemmung. Lesen Sie etwas mehr hierüber in einem eigenen Kapitel über Kombinationsbehandlung am Ende dieses eBooks. Ebenfalls im Kapitel über Kombinationsbehandlungen lesen Sie auch etwas über die Kombination von Aspirin® + anderen Gerinnungshemmern.
Dosierung
Aspirin®
Standarddosis zur Gerinnungshemmung: 100 mg tgl.
„Super-Aspirin“
Standarddosis für Clopidogrel: 75 mg tgl. In einigen dringlichen Fällen, wenn das Medikament schnell wirken muß, gibt man 300 mg Clopidogrel, um den Körper mit dem Medikament schnell „aufzuladen“.
Nebenwirkungen
Aspirin®
- Die häufigste Nebenwirkung betrifft Magen und Darm. Dabei kann es zu Magengeschwüren kommen, es können aber auch z.T. starke Blutungen aus dem Magen oder dem Darm kommen.
Diese Nebenwirkungen treten bei regelmäßiger Einnahme mit zunehmender Dosis häufiger auf, z.B. bei denjenigen Medikamentendosen, die man zur Behandlung von Schmerzen (300 mg tgl.) einsetzt.
Magen-Probleme sind hier oft der Grund zum Abbruch der Behandlung. Bei der zur Gerinnungshemmung üblichen Dosis von 100 mg sind die Magen-Darm-Probleme aber eher selten.
- Überempfindlichkeit: Sie tritt bei etwa 1 - 2% aller Menschen auf, die Aspirin® oder ein „Super-Aspirin“ einnehmen.
In Erscheinung tritt sie in Gestalt von Hautausschlag, aber auch gefährliche Schwellung des Kehlkopfes oder eine allgemeine schwere allergische Reaktion (Anaphylaxie) können auftreten. Besonders anfällig über Überempfindlichkeitsreaktionen sind Menschen mit Asthma und chronischer Nasennebenhöhlenentzündung.
- REYE-Syndrom: Es handelt sich um eine Schädigung des Gehirn und der Leber, das meistens bei Kindern im Alter von 4 - 9 Jahren auftritt, jedoch in allen Altersstufen vorkommen kann.
Das REYE-Syndrom ist selten, endet in etwa 25% tödlich und kann bei 30% der Betroffenen Schäden wie Sprach- und Lernschwierigkeiten hinterlassen.
Die Krankheit tritt im Durchschnitt 1 Woche nach dem Abklingen eines Virus-Infektes (z.B. Grippe, grippaler Infekt oder Windpocken) auf. Da die Symptome der Virusinfekte (z.B. Kopfschmerzen oder Fieber) oft mit Aspirin® behandelt werden nimmt man einen Zusammenhang des REYE-Syndroms mit der Aspirin®-einnahme an.
- Hirnblutung: Sie treten unter der Gabe von Thrombozytenaggregationshemmern häufiger auf als bei Menschen, die diese Medikamente nicht einnehmen, sind aber insgesamt selten.
„Super-Aspirin“
- Clopidogrel wird in Form einer inaktiven Medikamenten Vorstufe eingenommen, die im Körper durch das sog. CYP2C19-Enzym in seine aktive Form überführt wird. Andere Medikamente, die dieses Enzym beeinflussen (z.B. das Magenmittel Omeprazol) können daher die gerinnungshemmende Wirkung des Clopidogrels abschwächen und sollten daher nur sehr zurückhaltend zusammen mit Clopidogrel eingenommen werden.
- Bestimmte Schmerz- und Entzündungsmittel (z.B. Ibuprofen, Diclofenax, Dolormin®, Celecoxib oder Arcoxia®) blockieren ebenso wie Clopidogrel den ADP-Rezeptor auf der Thrombozytenoberfläche. Daher kann es gleichzeitiger Einnahme von Clopidogrel und solchen Medikamenten zu starken Blutungen kommen.
- Antidepressiv wirksame Medikamente können z.T. zu einer Funktionsstörung der Thrombozyten führen, sodaß die gleichzeitige Einahme von Clopidogrel mit Antidepressiva ebenfalls zu verstärkten und vermehrten Blutungen führen können.
Darf nicht gegeben werden
- bei Menschen, die auf Acetylsalicylsäure oder Clopidogrel allergisch sind dürfen diese Medikamente natürlich nicht einnehmen.
- Menschen, die allergisch sind auf Ibuprofen oder Menschen mit Asthma sollten Aspirin® zurückhaltend einnehmen.
- Ebenfalls vermieden sollte Aspirin® oder „Super-Aspirin“ bei Menschen, die zu Magengeschwüren neigen, die noch andere Gerinnungshemmer (z.B. Marcumar®) einnehmen oder bei denen eine angeborene Blutgerinnungsstörung bekannt ist.
- Keinesfalls dürfen Aspirin® oder „Super-Aspirin“ von Menschen eingenommen werden, die eine REYE-Syndrom überstanden haben.
Überwachung
Eine Laborüberwachung ist unter einer Behandlung mit Aspirin® oder „Super-Aspirin“ nicht notwendig.
Maßnahmen bei Überdosierung
Symptome einer Überdosierung von Aspirin® oder dem „Super-Aspirin“ sind:
- Schwindel
- Schläfrigkeit
- Übelkeit
- Erbrechen
- schnelle Atmung
- Übersäuerung des Bluts (Aspirin® enthält als Wirkstoff Acetylsalicylsäure)
- Krampfanfälle und
- Koma.
Zur Behandlung setzt man medizinische Aktivkohle ein und Infusionslösungen, um der Übersäuerung des Blutes entgegen zu wirken.
Ebenfalls gibt man Medikament zur Förderung der Urinausscheidung. Sowohl bei einer Aspirin®- als auch einer Clopidogrel-Vergiftung kann die Infusion von Thrombozyten-Konzentraten (spezielle Art von Bluttransfusionen) hilfreich sein. Das Problem bei einer solchen Transfusion besteht allerdings darin, daß auch geringe Restmengen von Aspirin® bzw. dem „Super-Aspirin“ im Blut die Funktion auch der neu gegebenen Blutplättchen hemmt.
Vitamin K-abhängige Medikamente (z.B. Marcumar®)
Anders als in Amerika und anderen Ländern ist in Deutschland der Wirkstoff Phenprocoumon die am häufigsten eingesetzte Substanz. Das bekannteste Medikament mit diesem Inhaltsstoff ist in Deutschland das Marcumar®, weshalb ich im folgenden immer Marcumar® schreibe, wenn ich Phenprocoumon meine.
Wirkweise
 |
| Abb.5 |
Wie Sie eingangs dieses eBooks schon gelesen haben entsteht ein Blutgerinnsel mit Hilfe zahlreicher Gerinnungsfaktoren, die aufeinander abgestuft mit- und aufeinander reagieren (Gerinnungskaskade, Abb. 5).
Sie werden in der Leber gebildet, wobei einige dieser Gerinnungsfaktoren (Faktoren 2, 7, 9 und 10) Vitamin K zur ihrer Synthese benötigen.
Substanzen wie das Phenprocoumon blockieren die Wirkung des Vitamin K bei der Synthese der hiervon abhängigen Gerinnungsfaktoren. Die hergestellte Menge dieser Faktoren (2, 7, 9 und 10) nimmt dadurch ab und steht in der Gerinnungskaskade nicht mehr zur Verfügung.
Dieser Mangel an Faktoren macht sich am Ende der Kaskade bemerkbar, wenn Prothrombin nicht mehr in Thrombin und damit kein Fibrinogen mehr in Fibrin umgewandelt werden kann, sodaß letztlich keine Fibrinfäden und damit kein Thrombus entsteht.
Substanzen wie das Phenprocoumon hemmen daher die Entstehung von Blutgerinnseln oder (anders herum formuliert:) sie hemmen die Blutgerinnung. Sie werden daher „Antikoagulanzien“ genannt („Anti“ bedeutet „gegen“ und „koagulanz“ bedeutet „Blutgerinnung“).
Aus dieser Wirkweise können Sie 4 wichtige Informationen entnehmen:
- Marcumar® kann keine bereits vorhandenen Blutgerinnsel auflösen, sondern nur verhindern, daß sich neue Gerinnsel bilden.
- Wenn man eine sehr große Menge Marcumar® einnimmt entsteht keinerlei Vitamin K-abhängiger Gerinnungsfaktor mehr und das Blut wird ungerinnbar.
- Wenn man die Wirkung des Marcumar® aufheben möchte führt man dem Körper einfach eine große Menge von Vitamin K zu. Weil eine bestimmte Menge an Marcumar® nur eine bestimmte Menge an Vitamin K blockieren kann wird die Marcumar®-Wirkung hierdurch aufgehoben. Weil die Bildung neuer Gerinnungsfaktoren aber Zeit benötigt wird die Wirkung des Vitamin K niemals sofort, sondern erst nach einigen Stunden oder sogar Tagen einsetzen.
- Weil vor der Wirkung des Marcumar® erst die noch im Blut vorhandenen Gerinnungsfaktoren verbraucht werden müssen beginnt die Wirkung des Marcumar® erst etwa 24 Stunden nach der Einnahme der 1. Tablette. Seine vollständige Wirkung entfaltet es, wenn man es weiter einnimmt, nach etwa 72 – 96 Stunden.
Wenn man die Marcumar®-Behandlung beendet wirkt es etwa 2 – 5 Tage nach, bevor sich die Blutgerinnung wieder völlig normalisiert hat. Es ist daher notwendig, das Medikament ohne Pausen durchgehend so einzunehmen, wie der Arzt es vorschreibt (siehe unten). Nimmt man es unzuverlässig und nicht regelmäßig verliert es im Laufe der Zeit seine Wirkung, nimmt man zuviel wird das Blut nicht mehr gerinnbar, was gefährlich werden kann.
Medikamente
Medikamente mit dem Wirkstoff Phenprocoumon sind z.B.
- Falithrom®
- Marcumar®
- Marcuphen®
- Phenpro® oder
- Phenprogamma®
Geschichte
Der Wirkstoff wurde 1939 entdeckt, nachdem in Amerika Vergiftungen an Kühen auftraten, die auf der Weide gestanden hatten und verblutet waren. Als Ursache fand man die Verunreinigung des Futters mit Süßklee, in dem die Substanz Cumarin entdeckt wurde. In der weiteren Folge fand man 42 verwandte chemische Substanzen, die die Blutgerinnung hemmten.
 |
| Abb.6 |
| Werbung als Rattengift |
Eine amerikanische Firma, die sich mit Ungezieferbekämpfung beschäftigte (Wisconsin Alumni Research Foundation) ließ sich einen dieser Wirkstoffe 1948 als Rattengift patentieren; aus dem Firmennamen wurde auch die bis heute gebräuchliche Bezeichnung des Wirkstoffes in Amerika „Warfarin“ abgeleitet.
In den 50er Jahren begannen Wissenschaftler damit, die Wirkung dieser Substanzen am Menschen zu erforschen. Die Substanz wurde allerdings zunächst nicht in der ärztlichen Behandlung eingesetzt, weil man die Hemmung der Blutgerinnung für unwiderruflich und tödlich hielt und man keine Erfahrung mit der Dosierung hatte.
Erst als ein Seemann 1951 mit der Substanz Selbstmord begehen wollte und überlebte lernte man, daß die tödliche Wirkung des Medikamentes aufgehoben werden konnte und begann, sich intensiver mit dem Einsatz am Menschen zu beschäftigen.
Der Durchbruch kam 1954, als man den amerikanischen Präsidenten Dwight D. Eisenhower wegen eines schweren Herzinfarktes mit dem Warfarin behandelte und retten konnte. (Ganz nebenbei: Es wird immer wieder spekuliert, daß Joseph Stalin nicht einem Schlaganfall bzw. einer Hirnblutung, sondern einer Vergiftung mit Warfarin zum Opfer fiel.)
Heute gehören Medikamente wie das Marcumar® zu den am häufigsten verschriebenen Medikamenten, allein in Amerika nehmen über 2 Millionen Menschen dieses Medikament ein.
Gründe für den Einsatz
Die häufigsten Gründe, Marcumar® einzunehmen sind:
- Tiefe Beinvenenthrombose
Hier entstehen Blutgerinnseln in den tief gelegenen, dicken Venen der Beine und des Beckens. Das Marcumar® verhindern, daß sich größere Gerinnsel bilden, die dann zu Lungenembolien (siehe unten) führen können.
- Lungenembolie
Dies ist eine Krankheit, bei der sich Blutgerinnsels aus den Bein-, Becken- oder Bauchvenen losreißen und dann mit dem Blutstrom in die Arterien der Lungen schwimmen, wo sie zu einer Verstopfung der betroffenen Gefäße führen. Das Marcumar® soll verhindern, daß erneut Blutgerinnsel entstehen und sich die lebensgefährliche Lungenembolie wiederholen kann.
- Vorhofflimmern oder Vorhofflattern
Beim Vorhofflimmern kommt es zu einem mechanischen Stillstand der Vorkammern des Herzens.
Die Rhythmusstörung an sich ist kaum gefährlich. Der Stillstand der Vorkammern verhindert aber, daß das Blut aus den Ecken und Zipfeln der Vorkammern ausgemolken wird, sodaß es hier stehen bleibt. Weil stehen bleibendes Blut schnell gerinnen kann (geben Sie einmal einen Tropfen Blut auf den Tisch) können sich innerhalb der Vorkammern Blutgerinnsel bilden.
Auch diese Blutgerinnsel sind, für sich alleine betrachtet, nicht gefährlich, solange sie sich im Herzen befinden. Weil sich das Herz aber laufend bewegen muß können sich diese Blutgerinnsel losreißen und das Herz verlassen. Sie gelangen dann in den Kreislauf und können hier in verschiedene Organe gelangen, deren Gefäße sie verstopfen können (Embolie). Welches Organ betroffen ist wird nach dem Prinzip des russischen Rouletts entschieden.
Viele solcher Embolien können zu lebensbedrohlichen, aber irgendwie reparablen Störungen führen: Wenn das Gerinnsel zufällig in das Gehirn oder in eine Herzkranzader gelangt entstehen Schlaganfälle oder Herzinfarkte. Und diese Embolien können dann, selbst wenn man sie überlebt, lebenslange Behinderung und schwere Organschäden verursachen.
- Mechanische Herzklappenprothesen
Wie schon oben beschrieben können sich an solchen Herzklappenprothesen Gerinnsel bilden, die entweder zur Funktionsstörung der Prothese mit der Notwendigkeit zur erneuten Operation führen oder die wie die oben beschriebenen Embolien in den Blutkreislauf gelangen und hier nach dem Prinzip des russischen Rouletts zu Embolien führen.
Alle Menschen mit mechanischen Herzklappenprothesen müssen daher lebenslang mit Marcumar® behandelt werden.
Menschen, denen keine künstliche, sondern eine biologische Herzklappe eingepflanzt wurde können dagegen oft auf Marcumar verzichten, weil solche biologischen Klappenprothesen keine Neigung zur Bildung von Blutgerinnseln haben. Solche Klappenprothesen haben dafür aber andere Nachteile, über die ich hier aber nicht berichten möchte (Wenn Sie sich für Einzelheiten interessieren lesen sie die Infos über Herzklappenoperationen).
- Herzinfarkt
Manchmal müssen auch Menschen, die einen Herzinfarkt überstanden haben für eine vorübergehende Zeit oder lebenslang Marcumar® einnehmen, um die Gefahr eines erneuten Herzinfarktes zu mindern. Dies ist aber eher sehr selten.
- Bei einigen Menschen entstehen im Gefolge des Herzinfarktes aber Aussackungen der Herzkammer (sog. „Aneurysma“), in denen sich Gerinnsel bilden können. In einigen dieser Fälle ist eine lebenslange Marcumar®-Behandlung ebenfalls nötig.
- Menschen, die eine Bypass-Operation, eine Ballonerweiterung („PTCA“) oder einen Stent bekommen haben benötigen hingegen nur sehr selten eine Behandlung mit Marcumar® (Wenn Sie für weitere Einzelheiten interessieren lesen Sie die Infos über eine Bypass-Operation oder PTCA.)
- Schlaganfall
Wenn ein Schlaganfall durch eine Embolie, d.h. ein Blutgerinnsel, das in das Gehirn geschwommen ist, verursacht wurde ist meistens eine lebenslange Marcumar®-Behandlung notwendig, um einen erneuten Schlaganfall zu verhindern.
Das Gleiche gilt für den „Mini-Schlaganfall“ (sog. „TIA“, d.h. Transitorisch-ischämische Attacke, also eine vorübergehende Durchblutungsstörung des Gehirns infolge von Embolien). Auch hier muß manchmal lebenslang mit Marcumar® behandelt werden, um einem großen Schlaganfall vorzubeugen.
Oftmals ist bei dieser Krankheit allerdings Aspirin® ausreichend.
- Nach bestimmten Operationen
Hier ist das Risiko für die Entstehung von Blutgerinnseln an verschiedenen Stellen der Blutgefäße erhöht.
Dies betrifft z.B. große orthopädische Operationen.
Manche Menschen müssen nach einer solchen Operation vorübergehend mit Marcumar® behandelt werden, um die Entstehung von Blutgerinnseln in den Blutgefäßen zu verhindern.
- Manchmal wird der Arzt Marcumar® aus anderen als den hier genannten Gründen verordnen. Man sollte in diesen Fällen unbedingt mit dem Arzt über den Grund für diese Behandlung und damit über ihre Notwendigkeit sprechen, über die voraussichtliche Dauer und über die Stärke der Gerinnungshemmung (siehe unten).
Dosierung
Marcumar® wirkt bei jedem Menschen unterschiedlich. Daher gibt es keine „Standarddosis“, die für jeden Menschen gelten würde. Einige Menschen benötigen eine große Marcumar®-Menge und andere eine viel geringere, um denselben Effekt zu erzielen. Einige Menschen gelangen schnell in den therapeutischen Bereich, andere langsamer. Jeder Patient wird daher eine ganz individuelle Marcumar®-Menge einnehmen müssen, um „seinen“ therapeutischen Bereich zu erreichen und zu halten.
Viele Faktoren beeinflussen die Höhe des INR-Wertes: Die Eßgewohnheiten, eine Diät, andere Medikamente, die man einnehmen muß oder eine neu aufgetretene Krankheit (z.B. Erkältungskrankheit). Wegen dieser schwankenden Marcumar®-Wirkung ist es großer Bedeutung, daß man seinen INR-Wert regelmäßig bestimmen läßt (siehe unten). Für die meisten Krankheiten ist ein INR-Wert von 2.0 – 3.0 notwendig. Manchmal reicht aber auch ein INR-Wert von 1.5 bis 2.0 aus und manchmal, z.B. bei bestimmten Herzklappenprothesen müssen Werte von 2.5 – 3.5 erreicht werden.
Den richtigen Wert legt der Arzt für jeden einzelnen Patienten fest, wenn er darüber entscheidet, aus welchem Grund er Marcumar® einnehmen muß. Für die meisten Krankheiten sind nämlich die erforderlichen INR-Werte durch die nationalen und internationalen ärztlichen Fachgesellschaften festgelegt worden. Der Arzt entscheidet auch darüber, ob es spezielle Gegebenheiten der Krankheit oder des Körpers des Patienten gibt, von diesen Empfehlungen abzuweichen. Man sollte also mit dem Arzt nicht nur über die grundsätzliche Entscheidung, Marcumar® einnehmen zu müssen, sprechen, sondern auch über das Ausmaß der Gerinnungshemmung, d.h. über den INR-Zielwert.
Wenn der INR-Zielwert im einem Bereich von 2.0 – 3.0 liegen soll spricht man davon, daß er „im therapeutischen Bereich“ liegt.
Fällt der INR-Wert ab, z.B. auf 1.5 bedeutet dies, daß das Blut „zu dick“ ist und der Patient nicht ausreichend vor der Entstehung von Gerinnseln geschützt sind. Der Arzt wird dann vorübergehen eine höhere Marcumar®-Dosis verordnen, bis der Wert wieder im „therapeutischen Bereich“ liegt.
Liegt der INR-Wert zu hoch (z.B. 4.5) bedeutet dies, daß das Blut „zu dünn“ ist und daß das Risiko innerer Blutungen besteht. In diesen Fällen wird der Arzt eine geringere Marcumar®-Dosis oder sogar eine kurze Marcumar®-Pause verschreiben, bis der Wert wieder in den therapeutischen Bereich abgesunken ist.
Wechselwirkungen mit anderen Medikamenten
Marcumar® kann mit hunderten von Medikamenten reagieren, die man in der Apotheke gegen Rezept bekommt oder die man auch frei ohne Rezept kaufen kann. Solche Wechselwirkungen können dazu führen, daß der INR-Wert plötzlich ansteigt (was die Gefahr innerer Blutungen provoziert) oder abfällt (was den Verlust des Schutzes gegen Blutgerinnsel bedeutet).
Beispiele solcher Medikamente, die mit Marcumar® reagieren finden Sie unten aufgeführt.
| Verschreibungspflichtige Medikamente | Frei erhältliche Medikamente |
|---|---|
| Antibiotika | Aspirin, ASS |
| Schmerzmittel | Aleve® (Naproxen) |
| Antiepileptika | Ibuprofen (Schmerz-, Rheumamittel) |
| Antidepressiva | Magen-Übersäuerungsmittel (z.B. Maalox®, Alka-Selzer®) |
| Anti-Blutplättchen-Mittel (z.B. Plavix®, Iscover®, Efient®, Brilique®) | Vitamin C (mehr als 500 mg/Tag) |
| Diabetes-Medikamente | Vitamin E (mehr als 400 IU/Tag) |
| Magenmittel (z.B. Zantic®, Tagamet®) | Multivitamin-Präparate (enthalten oft Vitamin K) |
| Gicht-Medikamente (z.B. Allopurinol) | „Knochen- und Gelenk-Mittel“ (z.B. Glukosamin, Chondroitin) |
| Cholesterin-senkende Medikamente | Coenzym Q10 |
| Steroide (z.B. Hormone, Kortison) | |
| Schilddrüsen-Medikamente | |
| Mittel gegen Herzrhythmusstörungen | |
| Mittel gegen Pilzerkrankungen |
Die Liste ist keinesfalls vollständig; sie soll nur eine Vorstellung davon geben, wie auch ganz gewöhnliche Medikamente, über deren Einnahme man oft nicht weiter nachdenkt, zu einer Beeinflussung der Marcumar®-Therapie führen können.
Es ist von großer Bedeutung, daß man seinem Hausarzt über jedes Medikament berichtet, daß man einnehmen soll oder will, sei es, daß dieses Medikament von einem anderen Arzt verschriebenen wurde oder daß man es selber ohne Rezept gekauft haben.
Man muß als Marcumar®-Patient immer daran denken, daß auch Substanzen, die man vielleicht nicht als „richtiges“ Medikament ansieht (z.B. homöopathische Medikamente, Wellness- oder Anti-aging-Substanzen, Vitamine usw.) den INR-Wert verändern.
Wenn man Medikamente benötigt, die mit Marcumar® reagieren können, so bedeutet dies nicht, daß man entweder auf das betreffende Medikament oder auf Marcumar® verzichten müßte; es bedeutet vielmehr, daß man seinen INR-Wert häufiger kontrollieren lassen muß, um unerwartete Schwankungen besser und sicherer ausgleichen zu können.
Es ist wichtig zu wissen, daß die häufigsten Ursachen für eine unzureichende oder zu starke Wirkung des Marcumar® Neben- oder Wechselwirkungen mit anderen Medikamenten, Nahrungsmitteln oder (siehe unten) naturheilkundlichen Substanzen sind.
Wechselwirkungen mit natürlichen Wirkstoffen und Homöopathika
Auch Naturheilmittel oder Homöopathika können zu gefährlichen Wechselwirkungen mit Marcumar® führen. Man sollte daran denken, daß allein die „pflanzliche“ oder „natürliche“ Herkunft eines Medikamentes oder einer Substanz nicht automatisch bedeutet, daß sie sicher und ungefährlich ist.
Nachfolgend finden Sie eine Liste einiger Naturheilmittel und homöopathischen Medikamente, die die Marcumar®-Wirkung beeinflussen können.
| Agrimonia | Ginkgo | Pappel | Sellerie |
| Aloe | Griechisches Heu | Mutterkraut | Senega (= Klapperschlangenwurzel) |
| Angelica (Dong Quai) | Grüner Tee | Passionsfrucht | Silberkerze |
| Anissamen | Johanniskraut | Pau d’arco | Sommerspieren |
| Arnica | Kamille | Petersilie | Süßer Klee |
| Biloba | Kassie-Zwiebel | Pfeffer-Nessel | Süßer Waldmeister |
| Bitterklee | Knoblauch | Policosanol | Süßholz |
| Blasentang (Fucus) | Löwenzahn | Quassia | Tamarinde |
| Boldoblätter | Luzerne | Sarsaparille | Tonka-Bohne |
| Bromelain (Ananas) | Meerrettich | Schafgarbe | Wilde Karotte |
| Ecchinacea | Mistel | Schlehe | Wilder Kopfsalat |
Die Liste hat keinen Anspruch auf Vollständigkeit.
Wenn man Naturheilmittel oder Homöopathika einnehmen muß oder möchte sollte man vorher einen Homöopathen oder Arzt für Naturheilkunde danach befragen, ob Wechselwirkungen mit Marcumar bekannt sind. Und wenn man sich nicht sicher ist sollte man den INR-Wert häufiger testen lassen.
Ernährung, Diät und Marcumar®
Marcumar® blockiert (siehe oben) das Vitamin K, das man mit seiner Ernährung zu sich nimmt. Wenn man seinem Körper also viel Vitamin K zuführt wird die Wirkung des Marcumar® abgeschwächt, wenig Vitamin K in der Nahrung führt zu einer Wirkungsverstärkung des Marcumar®.
Den größten Gehalt an Vitamin K hat grünes Blattgemüse und Früchte wie Avocados oder Kiwis. Das bedeutet aber nicht, daß man, wenn man Marcumar®-Patient ist auf solches grüne Gemüse oder auf Früchte verzichten müsste. Grünes Gemüse enthält nämlich .................
-x-x-x-x-x-x-x